salmuera, desaladoras
La desalinización elimina sales de varios metales e impurezas del agua de mar . Se utiliza para obtener agua dulce para consumo humano y para uso doméstico/industrial.
11 agosto 2022.- Las sales extraídas y otros compuestos metálicos presentes en la mezcla de desalinización forman una mezcla hipersalina comúnmente conocida como salmuera. Este subproducto de desecho contiene principalmente cloruro de sodio (NaCl) y agua. Su composición depende del tipo de proceso de desalinización y de la zona donde se lleva a cabo la desalinización.
El crecimiento económico y la competitividad global de la Unión Europea requieren la disponibilidad de materias primas vitales de relevancia estratégica (materias primas críticas o CRM) para fortalecer el liderazgo industrial a largo plazo. La extracción de minerales a partir de salmueras hipersalinas generadas como subproductos de las plantas desaladoras de agua de mar ha despertado el interés de los científicos.
Unas 18.200 plantas desalinizadoras operan en todo el mundo con una capacidad global acumulada cercana a los 90 millones de m 3 /día [1]. Se espera que esta capacidad crezca a un ritmo cada vez más rápido en el futuro cercano debido a la crisis de escasez de agua en todo el mundo y al aumento de la demanda de agua [2].
La salmuera generada en la desalinización de agua de mar (SWD) se vierte actualmente al mar, generando impactos ambientales negativos y representando un peligro potencial para los ecosistemas marinos debido a su alta salinidad. Además, si se descarga la salmuera, se perderá la energía utilizada para su producción, así como el beneficio de utilizarla como fuente potencial de metales y metales críticos.
Sin embargo, para la recuperación de la salmuera se requiere mucha investigación. En particular, un proyecto europeo con el acrónimo SEA4VALUE está trabajando en cómo extraer metales y metales críticos minimizando el impacto ambiental negativo. La visión del proyecto es crear un proceso multimineral y modular para separar, concentrar y cristalizar molibdeno, magnesio, escandio, vanadio, galio, boro, indio, litio y rubidio en plantas desalinizadoras de agua de mar. Un primer desafío es la eliminación de las grandes cantidades de calcio de la salmuera. Otro tema es la cantidad de energía requerida.
¿Qué son los metales críticos y por qué la salmuera es una fuente potencial?
La escasez de algunos elementos está dando lugar a nuevas estrategias para satisfacer la creciente demanda industrial. Desde un punto de vista geoquímico, la mayoría de los elementos, excepto Al, Si, Fe, Ca, Mg, Na y K, son escasos en el sentido de que se extraen de minerales de media a alta ley que corren el riesgo de agotarse [3].
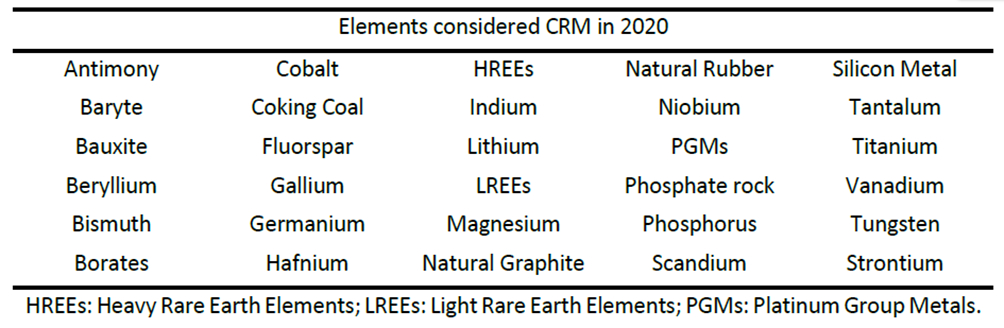
La lista de la Unión Europea de metales críticos (ver Tabla 1) destaca el interés político en estos elementos escasos [4]. Las razones detrás de la creciente preocupación por el suministro de los metales son su mayor uso social, el agotamiento de los recursos extraídos convencionales y la estabilidad política y económica de algunos de los principales productores.
Tabla 1. Lista de Materias Primas Críticas de la Unión Europea (2020) [4]. |
 |
Las estrategias utilizadas para paliar este problema han sido:
i) la explotación de minerales primarios de baja calidad,
ii) la “recuperación” de fuentes no convencionales como flujos de desechos industriales considerados como recursos secundarios, y
iii) la sustitución del material por un metal o elemento más fácilmente disponible o reducción, donde la cantidad de un metal o elemento necesario se reduce por un principio de co-sustitución.
Según Zimmermann et al. [5], el 30 % de todos los materiales críticos clasificados en la UE se desechan y muchos de ellos tienen índices de disipación superiores al 50 %.
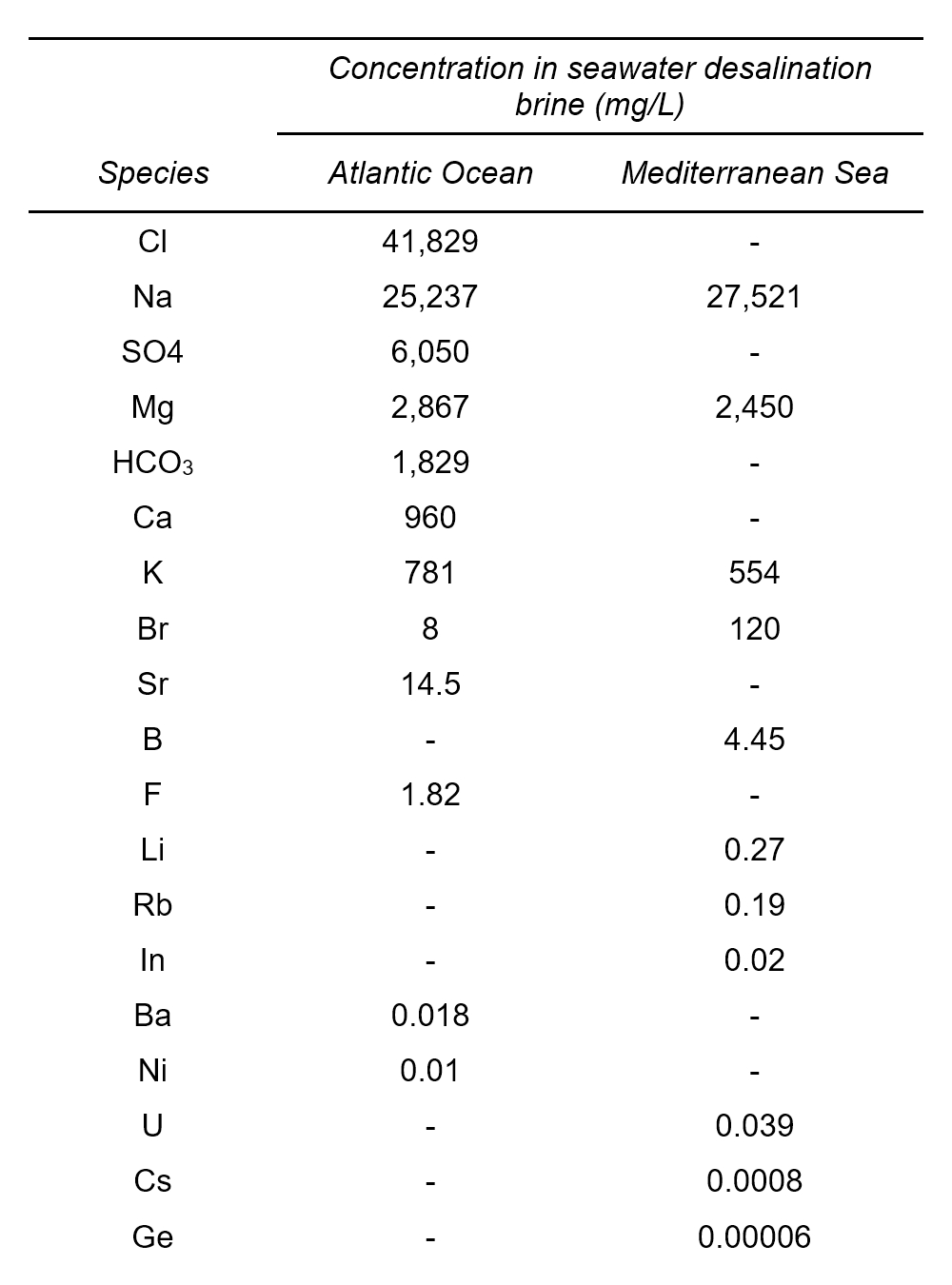
Las salmueras de desalinización de agua de mar por ósmosis inversa (SWRO), que son la mayoría de las salmueras SWD [2], son corrientes de desechos generadas en la producción de agua potable que contienen los componentes de la fuente en concentraciones más altas que el agua de mar inicial por un factor típicamente de dos ( ver Tab.2) [6].
Tabla 2 . Valores medios de elementos presentes en concentrados de ósmosis inversa de agua de mar [6]. |
 |
La capacidad mundial de desalinización prevista es bastante variable. Según las fuentes de las referencias [1] y [7], se puede prever que esté en el rango de 90-150 millones de m 3 por día, y se espera que siga creciendo según las predicciones de cambio climático [7].
El proyecto SEA4VALUE investigará la viabilidad de recuperar Li, B, Mg, Sc, V, Ga, Rb, Mo e In de las salmueras generadas en plantas SWD. Para lograr esto, se desarrollarán tecnologías innovadoras, que incluyen nanofiltración avanzada, cristalización por membrana, destilación avanzada de múltiples efectos y procesos selectivos como la adsorción y la extracción por solventes (ver Fig. 1).
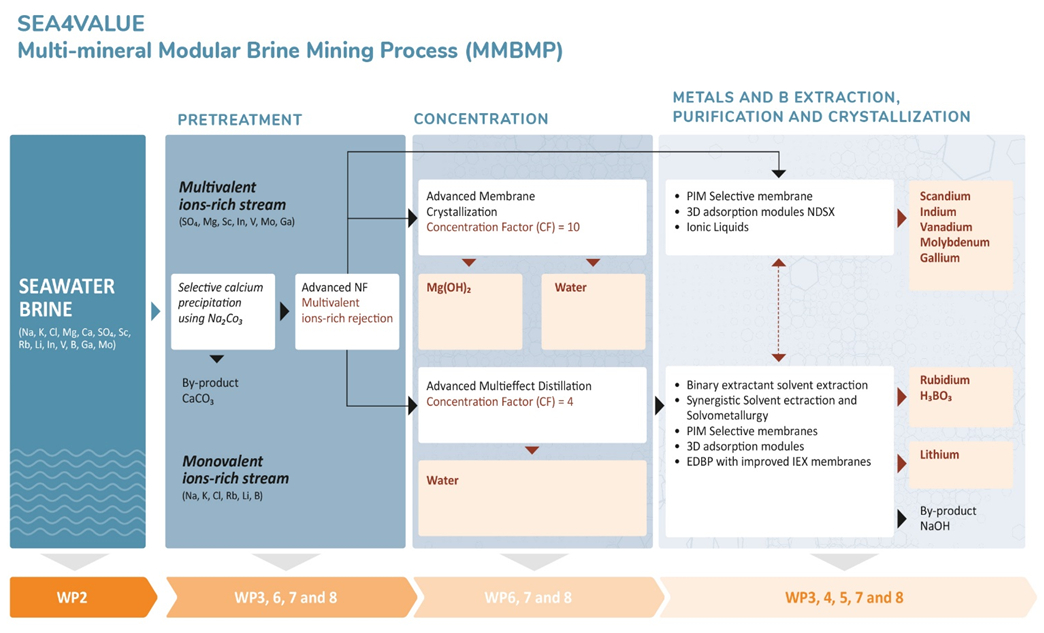 |
Figura 1. Esquema simplificado de los pasos del proceso para la recuperación de metales prevista en el proyecto SEA4VALUE. |
Beneficios de la eliminación de Ca de la salmuera
Una de las principales limitaciones asociadas con la recuperación de elementos críticos, que están presentes en niveles traza, de la salmuera de ósmosis inversa (OI) es la necesidad de eliminar los principales elementos principales, específicamente elementos divalentes como calcio-Ca(II) y magnesio-Mg(II). Dado que Mg es uno de los elementos objetivo en SEA4VALUE, debe separarse selectivamente de Ca, lo cual es un desafío.
Los valores de las concentraciones de Ca(II) en las salmueras de desalinización SWRO están en el rango de 700–900 mg(Ca)/L. Hay una doble necesidad de eliminación de Ca(II):
i) Ayuda a prevenir la formación de incrustaciones en la mayoría de las etapas de separación necesarias para recuperar los diferentes oligoelementos objetivo.
ii) Ayuda a mejorar los factores de selectividad de los oligoelementos, si están presentes como componentes mayoritarios en comparación con el Ca(II) restante.
Como se indicó, la eliminación de calcio es un pretratamiento obligatorio en el proyecto SEA4VALUE. La eliminación de Ca(II), en forma de precipitación de carbonato de calcio de las salmueras, fue revisada críticamente por Bond y Veerapaneni [8] junto con los procesos de desalinización. El uso de cristalizadores de lecho fluidizado para la producción de gránulos de carbonato de calcio [9], la influencia de los antiincrustantes utilizados en los procesos de desalinización de agua de mar por ósmosis inversa y la presencia de impurezas (p. ej., otros iones metálicos) en la precipitación de carbonato de calcio fueron los aspectos principales. a considerar [10].
Si bien la concentración de calcio en el agua de mar y el concentrado de desalinización es relativamente alta, la extracción de un producto de calcio vendible del agua de mar a nivel industrial ha atraído muy poca atención, con solo una notable excepción en una instalación de desalinización de agua salobre en el sur de California, EE.UU. [ 9].
Cabe mencionar que la extracción de Ca(II) a partir de agua de mar o concentrado en forma de sulfato de calcio (yeso), no ha recibido una atención significativa debido al bajo precio del yeso de grado comercial. Por ello, y además de considerar la mayor solubilidad de esta sal frente al carbonato cálcico, en el proyecto SEA4VALUE se descartó la precipitación de yeso [11,12]. Deben descartarse otras opciones, como el uso de intercambio iónico, ya que no es posible eliminar selectivamente el Ca(II) y el Mg(II) [13]. Todas estas consideraciones impulsaron el desafío de la eliminación selectiva de Ca como pretratamiento antes de los otros pasos del proceso, como se informa en la Figura 1 y se describe a continuación.
Eliminación separada de calcio y magnesio
El calcio y el magnesio son dos de los electrolitos más abundantes en el agua de mar y su recuperación por separado puede ser útil para diversas aplicaciones. En el proyecto SEA4VALUE, un primer resultado es la recuperación de calcio como carbonato de calcio, mientras que se prevé que el magnesio se recupere como hidróxido de magnesio en etapas sucesivas del proceso. Cada uno de estos elementos tiene varios usos [14,15].
Para permitir una separación selectiva, se utilizó la diferente reactividad de Ca y Mg debido a su diferente hidratación. Los iones de magnesio están más hidratados que los iones de calcio [16], lo que conduce a una menor capacidad para combinarse con iones negativos, como el ion carbonato. Esto conduce a una precipitación de carbonato de calcio más fácil en comparación con el carbonato de magnesio [17,18].
Sin embargo, el magnesio en salmuera es cinco veces más concentrado que el calcio, lo que induce una tasa de crecimiento reducida de calcita (una forma cristalina de carbonato de calcio) como observaron varios investigadores [19–21]. Como resultado de la mayor concentración de Mg en comparación con la concentración de Ca, el magnesio puede dificultar la cristalización de la calcita, pero esto depende de las condiciones de operación, como se muestra a continuación.
Se llevaron a cabo experimentos con soluciones que simulaban una salmuera promedio a diferentes pH, temperatura, fuerza iónica y proporciones molares de carbonato/ion de calcio (R) para intentar aumentar la precipitación de calcio minimizando la eliminación de magnesio (consulte [18] para obtener resultados detallados). Un parámetro de particular interés fue la temperatura, ya que su aumento permitió aumentar la tasa de crecimiento de la calcita, como se muestra en la Figura 2 utilizando una solución que contenía cationes Ca y Mg.
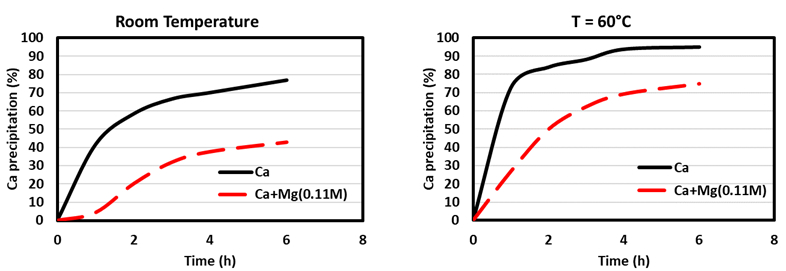 |
Figura 2. Efecto del Mg(II) sobre la precipitación de Ca(II) a (a) temperatura ambiente y (b) 60 °C (elaborado a partir de [18]). |
Se puede observar que a temperatura ambiente, el efecto del Mg sobre la precipitación de Ca es más pronunciado que a temperatura más alta. Además, a temperaturas más altas, se observa un aumento de la precipitación de Ca. Posteriormente, una solución de salmuera simulada (SB) arrojó una precipitación de Ca de alrededor del 85 %, mientras que la coprecipitación de Mg fue de alrededor del 7 % (ver Fig. 3).
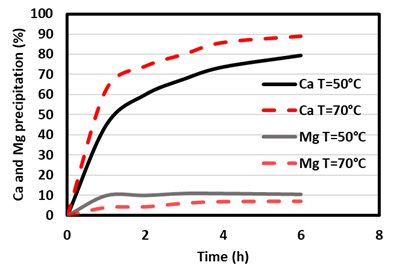 |
Figura 3. Efecto de la temperatura sobre la precipitación de Ca y Mg en la solución de SB (pH NaHCO3 = 9.0 y R = 3; elaborado a partir de [18]). |
Cómo la integración entre experimentos y modelado puede ayudar a la investigación
El modelado químico es una poderosa herramienta utilizada para simular procesos químicos desde una perspectiva termodinámica. El modelado se puede utilizar para predecir la precipitación de calcio en diferentes condiciones, lo que reduce el costo de los experimentos al definir las condiciones óptimas. Sin embargo, la simulación de procesos a alta fuerza iónica requiere modelos específicos. Se pueden usar diferentes códigos y software para modelar procesos a alta fuerza iónica, por ejemplo, OLI y PhreeqC , los cuales se usan en SEA4VALUE.
Para analizar la precipitación de carbonato de calcio se ha utilizado un modelo termodinámico en forma de código PhreeqC que se apoya en el cálculo de los coeficientes de actividad y los índices de saturación mineral (SI) [22]. Debido a la alta salinidad de las soluciones, se utilizó la base de datos de Pitzer , y fue necesario extenderla a elementos convencionalmente despreciados por sus bajos contenidos en salmuera (mg/kg a μg/kg) que ahora se consideran en la identificación de alternativas recursos minerales.
Utilizando la composición inicial de la salmuera de agua de mar de OI y considerando la información de los ensayos de precipitación experimental, se simuló la variación de las concentraciones de solutos mayoritarios y minoritarios tanto en la salmuera como en las fases sólidas con el código numérico PhreeqC (v3.6.2) [23]. Encontrar el porcentaje de remoción de Ca en función de la concentración de bicarbonato fue el principal objetivo de la etapa de modelado, y la validación del esfuerzo de modelado se llevó a cabo utilizando los datos experimentales generados en las reacciones de precipitación.
Como puede verse en la Figura 4, los valores experimentales concuerdan bien con los predichos por PhreeqC. Luego, el código numérico se puede usar para optimizar la eliminación de Ca(II) en términos de niveles de carbonato total y pH para evitar la posible coprecipitación de Mg(II).
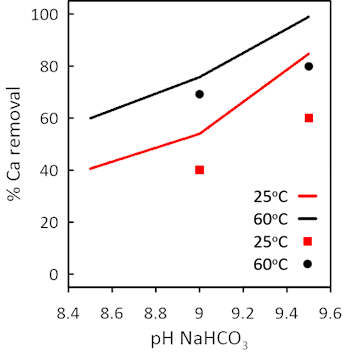 |
Figura 4. Comparación de modelos (líneas continuas) y datos experimentales (puntos cuadrados y rombos) en la precipitación de Ca(II) en función del pH inicial (elaborado a partir de [18]). |
Cómo puede contribuir la nanofiltración a una mayor recuperación de agua y oligoelementos
Después de la eliminación de Ca(II), la salmuera rica en Mg(II), que también contiene oligoelementos específicos para recuperar, podría someterse a una etapa de separación basada en el uso de membranas de nanofiltración (NF) (ver Fig. 5) . Las membranas NF basadas en una capa activa de poliamidas semiaromáticas (p. ej., de DuPont) han mostrado altos valores de rechazo (>80 %) para iones multivalentes (p. ej., Ca(II), Mg(II), Sr(II) y sulfatos) y bajos valores de rechazo para los iones monovalentes (Na, K, Cl) y la mayoría de los elementos traza específicos que se recuperarán. El uso de NF puede verse como una etapa de prepurificación de la salmuera para eliminar aquellos iones que afectan las etapas de tratamiento del proceso posterior.
 |
Figura 5. Montaje experimental con membrana de nanofiltración para la evaluación de la prepurificación de salmuera; (b) detalle de una celda de prueba de membrana de hoja plana. |
La nanofiltración ha sido postulada por Telzhensky et al. [24] y Reig et al. [25] como un paso de pretratamiento de salmuera para producir concentrados ricos en Mg(II) y Ca(II) o Mg(OH) 2 (s). El rechazo de iones polivalentes se probó con una nueva familia de membranas NF, donde la capa activa se ha modificado utilizando una tecnología de deposición capa por capa (LBL). Por lo general, en una deposición de LBL, los polielectrolitos de alto peso molecular se adsorben en la capa activa de una membrana.
El rechazo generalmente aumentó con la presión en el rango estudiado (desde 8 hasta 20 bar). También aumentó el rechazo de NaCl no deseado, alcanzando un máximo del 12 % a 20 bar. Sin embargo, los iones divalentes se rechazaron más fácilmente que el NaCl, por lo que se logró el objetivo de NF. El rechazo de los iones mayoritarios se estabilizó con el aumento de la presión, alcanzando una meseta a presiones de 18 bar. El orden de rechazo con salmuera SWD-RO a 20 bar fue Al(III) > S(VI) > Mg(II) > Sr(II) > Cu(II) > Ca(II) > Ni(II) > NaCl > K (YO).
NF270 es una membrana cargada negativamente, por lo que se observaron mayores rechazos para los aniones, con la excepción de Al(III). Como ión trivalente, el mecanismo de exclusión dieléctrica explica su mayor rechazo que los iones divalentes o monovalentes. La exclusión dieléctrica es causada por las interacciones de los iones con las cargas eléctricas unidas inducidas por los iones en las interfaces entre medios de diferentes constantes dieléctricas. Se considera uno de los mecanismos de nanofiltración. La presencia de una carga eléctrica fija de magnitud apreciable en la superficie de la membrana puede provocar un fuerte apantallamiento de exclusión dieléctrica, es decir, cuanto mayor sea la carga del ion, mayor será su rechazo.
La concentración inicial de un ion juega un papel importante en su grado de rechazo. Cuando se utilizan salmueras altamente concentradas, ocurre un fenómeno de pantalla (cruce selectivo de iones a través de la membrana) en la capa superficial de la membrana activa y se minimiza el efecto Donnan (distribución no simétrica de partículas cargadas a través de los dos lados de la membrana). Los contraiones filtran la carga de la capa superficial de la membrana y, en consecuencia, el tamizado se convierte en el mecanismo dominante para el rechazo de especies iónicas. Los iones con un radio hidratado más pequeño, como Na(I) y K(I), se rechazan con menos facilidad de la salmuera que los otros iones, como los iones multivalentes.
Cómo se puede usar la eliminación de calcio de la salmuera para desarrollar un proceso con descarga de líquido casi nula
Dado que se requiere una temperatura de salmuera de 60 a 70 °C para eliminar el calcio, la salmuera descargada del sistema de ósmosis inversa debe calentarse a este rango de temperatura. Esto debería hacerse, por ejemplo, con la ayuda de colectores solares para aumentar la sostenibilidad del proceso. Luego, el Ca se elimina por precipitación a pH controlado.
Dado que una operación de destilación por membrana (MD) se basa en la diferencia de temperatura entre una corriente caliente y una corriente fría, una etapa posterior basada en MD podría aprovechar la alta temperatura.
El bajo contenido de Ca reduce la formación de incrustaciones en la membrana generalmente asociadas con minerales a base de calcio. Por lo tanto, el flujo de agua no disminuirá significativamente y se mejorará la eficiencia operativa y económica de la destilación por membrana. En consecuencia, el proceso de valorización de la salmuera se puede mejorar mediante el desarrollo de un proceso caracterizado por una descarga de líquido cercana a cero (NZLD), donde se recuperan casi todos los componentes contenidos en la salmuera (agua y sales).
De la unidad MD se recupera agua y, tras la remineralización, se obtiene agua potable. La mezcla concentrada de los diversos elementos que inicialmente estaban presentes en el agua de mar en muy baja concentración se envía a recuperación de sal (ver Fig. 6). En esta mezcla, el Mg(II) es el componente principal, junto con NaCl y elementos menores.
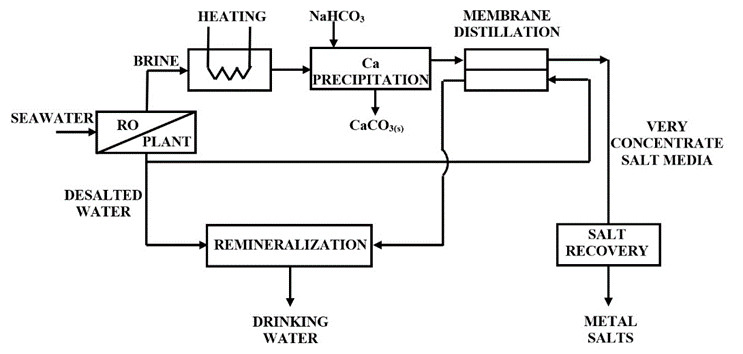 |
Figura 6. Esquema conceptual de la valorización de la salmuera después de la eliminación previa de Ca para acercarse a NZLD [18]. |
Conclusión y perspectiva
La investigación sobre tecnologías y procesos que pueden aprovechar la salmuera como fuente de metal está completamente abierta y, hasta donde sabemos, el enfoque de la precipitación selectiva de calcio como se describe aquí ha sido estudiado solo por Wang et al. [26], quienes obtuvieron resultados comparables trabajando a una temperatura (85 °C) superior a las que investigamos (hasta 70 °C). El esquema de procesamiento (ver Fig. 6) es un ejemplo de un proceso limpio que fue posible diseñar después de recopilar información para comprender profundamente los fundamentos de uno de los procesos químicos involucrados.
El estudio de los aspectos químicos de la eliminación de calcio de la salmuera integra aspectos teóricos, es decir, modelado de salmuera con códigos de equilibrio geoquímico como PhreeqC, y esfuerzos experimentales. El uso de carbonato ácido de sodio redujo la pérdida de Mg durante la precipitación de CaCO 3(s) porque el pH se controló a un valor inferior al de la precipitación con hidróxido de magnesio.
Los resultados generales (pH 9,0, temperatura de 60–70 °C, relación molar HCO 3 – /Ca = 3, eficiencia de eliminación de Ca superior al 90 % con una pérdida de Mg de alrededor del 7 %) son de interés potencial para diseñar un proceso NZLD para tratamiento de valorización de salmueras.
Un cuello de botella de la configuración que se muestra en la Figura 6 es la necesidad de calentar la salmuera a 60–70 °C. Se requiere una gran cantidad de energía considerando tanto el alto caudal de salmuera como la temperatura necesaria durante el proceso de precipitación de carbonato de calcio.
Otro enfoque que puede ser más sostenible desde el punto de vista energético, que también se exploró como parte del proyecto SEA4VALUE, es operar a una temperatura más cercana a la temperatura ambiente. Esto es más fácil de controlar y mantener. Se planean pruebas en una planta piloto de laboratorio que opere en el sitio, y los resultados deberían estar disponibles dentro de algunos años.
Fuentes:
[1] International Desalination Association, idadesal.org. (accessed on April 29, 2022)
[2] M. Badruzzaman et al., Selection of pretreatment technologies for seawater reverse osmosis plants. A review, Desalination 2019, 449, 78–91. https://doi.org/10.1016/j.desal.2018.10.006
[3] M. L. Söderman et al., in Syst. Perspect. Electromobility, B. A. Sandén (Ed.), Chalmers University of Technology, Gothenburg, Sweden, 2014, 76–89.
[4] European Commission, Study on the EU’s list of Critical Raw Materials (2020): Final Report, 2020. https://doi.org/10.2873/11619
[5] T. Zimmermann, Uncovering the fate of critical metals: tracking dissipative losses along the product life cycle, J. Ind. Ecol. 2017, 21, 11981211. https://doi.org/10.1111/jiec.12492
[6] P. Loganathan et al., Mining valuable minerals from seawater: A critical review, Environ. Sci. Water Res. Technol. 2017, 3, 37–53. https://doi.org/10.1039/c6ew00268d
[7] E. Jones et al., The state of desalination and brine production: a global outlook, Sci. Total Environ. 2019, 657, 1343–1356. https://doi.org/10.1016/j.scitotenv.2018.12.076
[8] R. Bond, S. Veerapaneni, Zero Liquid Discharge for Inland Desalination, Black and Veatch, 2007.
[9] W. Shih et al., Chino II Desalter concentrate management via innovative by-product resale and treatment, American Membrane Technology Association, San Antonio, TX, 2013.
[10] L .F. Greenlee et al., Effect of antiscalant degradation on salt precipitation and solid/liquid separation of RO concentrate, J. Membr. Sci. 2011, 366, 48–61. https://doi.org/10.1016/j.memsci.2010.09.040
[11] F. Alimi et al., Kinetics of the precipitation of calcium sulfate dihydrate in a desalination unit, Desalination 2003, 158, 9–16. https://doi.org/10.1016/S0011-9164(03)00426-0
[12] R. Sheikholeslami, H. W. K. Ong, Kinetics and thermodynamics of calcium carbonate and calcium sulfate at salinities up to 1.5 M, Desalination 2003, 157, 217–234. https://doi.org/10.1016/S0011-9164(03)00401-6
[13] J. E. Goldman et al., Selective Salt Recovery from Reverse Osmosis Concentrate. Report Foundation, W.R.-61, 2013.
[14] Major Industrial Applications uses of CaCO3 calcium carbonate in everyday life, usmasterbatch.com. (accessed on March 2, 2022)
[15] Uses Of Magnesium Hydroxide, www.osianmcpl.com. (accessed on March 2, 2022)
[16] P. Silvestroni (Eds.: M. Pasquali, A. Latini), Fondamenti di Chimica, CEA, 2020. ISBN: 9788808920539
[17] C. Akilan et al., Temperature effects on ion association and hydration in MgSO4 by dielectric spectroscopy, ChemPhysChem 2006, 7, 2319–2330. https://doi.org/10.1002/cphc.200600342
[18] R. Molinari et al., Selective precipitation of calcium ion from seawater desalination reverse osmosis brine, J. Cleaner Production 2021, 329, 129645. https://doi.org/10.1016/j.jclepro.2021.129645
[19] T. Chen et al., Influence of Mg2+ on CaCO3 formation-bulk precipitation and surface deposition, Chem. Eng. Sci. 2006, 61, 5318–5327. https://doi.org/10.1016/j.ces.2006.04.007
[20] Y. Zhang, R. A. Dawe, Influence of Mg2+ on the kinetics of calcite precipitation and calcite crystal morphology, Chem. Geol. 2000, 163, 129–138. https://doi.org/10.1016/S0009-2541(99)00097-2
[21] Y. Choi et al., Effect of chemical and physical factors on the crystallization of calcium sulphate in seawater reverse osmosis brine, Desalination 2018, 426, 78–87. https://doi.org/10.1016/j.desal.2017.10.037
[22] K. S. Pitzer, The Treatment of Ionic Solutions over the Entire Miscibility Range, Ber. Bunsengesellschaft Phys. Chemie. 1981, 85, 952–959. https://doi.org/10.1002/bbpc.19810851107
[23] D. L. Parkhurst, C. A. J. Appelo, Description of Input and Examples for PHREEQC Version 3 – A Computer Program for Speciation, Batch-Reaction, One-Dimensional Transport and Inverse Geochemical Calculations, U.S. Geological Survey Techniques and Methods 2013, 6, A43, 497.
[24] M. Telzhensky et al., Selective separation of seawater Mg2+ ions for use in downstream water treatment processes, Chem. Eng. J. 2011, 175, 136–143. https://doi.org/10.1016/j.cej.2011.09.082
[25] M. Reig et al., Integration of nanofiltration and bipolar electrodialysis for valorization of seawater desalination brines: Production of drinking and waste water treatment chemicals, Desalination 2016, 382, 13–20. https://doi.org/10.1016/j.desal.2015.12.013
[26] Y. Wang et al., Selective removal of calcium ions from seawater or desalination brine using a modified sodium carbonate method, Desal. Water Treat. 2020, 174, 123–135. https://doi.org/10.5004/dwt.2020.24828
[27] Morillo, J., Usero J., Rosado D., El Bakouri, H. Comparative study of brine management technologies for desalination plants, March 2014. Universidad de Sevilla, Universidad de Kiel, Abengoa. DOI:10.1016/j.desal.2013.12.038
Autores
Raffaele Molinari*1, Ahmet Halil Avci1, Pietro Argurio1, Efrem Curcio1, Sandra Meca2, Sandra Casas2, Mireia Plà-Castellana2, Hannah Arpke2, Jose Luis Cortina3
1 Department of Environmental Engineering (DIAm), University of Calabria, via P. Bucci, cubo 44/A, Rende (CS), Italy.
2 Sustainability Area, EURECAT, Centre Tecnològic de Catalunya, Spain
3 Chemical Engineering Department, Universidad Politécnica de Cataluña · Barcelona Tech (UPC), Spain




















COMENTARIOS